摘要:叩开被尘封的我国生理学先驱者们开创“肠抑胃素(entrogastrone)” 的历史记忆,正视随之脱胎的“瘦素(Leptin)”方兴未艾,掠影现代肠胃激素发展轨迹中诸多科研成果亮点,探寻原始创新的孕育生态与科学卫道精神的内在自我秉持。
1 湍流涌动促新说:肠促胰液素的发现和内分泌学的兴起
人类对消化过程的兴趣可追述到数千年前。早在春秋战国时期成书的《黄帝内经?素问》中就有对消化系统的记载:“六腑者,传化物而不藏,故实而不能满也。所以然者,水谷人口,则胃实而肠虚。食下,则肠实而胃虚”。
16世纪,欧洲Vesalius对胃的首次解剖,开启了人类对胃内食糜化学成分的研究。此后的一个多世纪,对于胃中酸性液体的来源有各种各样的猜测。解剖学家Paracelsus认为胃液源于摄入的酸性水;Albrecht von Haller在《Elementa Physiologiae Corporis Humani》一书中却另有其说:胃液源于降解的食物。19世纪初,盐酸被确认是胃液的主要成分。 1829年,Beaumont在《Physiology of Digestion》中首次描述了一个胃瘘患者在摄食后胃液由胃自身分泌的现象[1]。
随后,胃液分泌和调节机制成为学界关注的焦点。19世纪末,现代消化生理学的奠基人巴浦洛夫(I. P. Pavlov)采用假饲(sham-feeding)实验证明:迷走神经控制了胃液的分泌。自此,迷走神经切除术即被成功地用于对胃液过多症和胃溃疡患者的治疗。在此基础上,巴浦洛夫提出的“神经论(nervism)”—即消化液的分泌完全由神经活动支配的理论,成为19世纪末到20世纪初在消化液分泌和调节机制研究中占统治地位的理论学说,他被授予1904年的诺贝尔生理学奖。
1901年,伦敦大学的两位生理学家Bayliss和Starling发现,将盐酸溶液注入狗的上段小肠时,会引起胰液分泌。而无论是使用中等剂量的阿托品阻断交感神经,还是直接切除狗小肠周围的神经,都不能阻止这种生理反应。这个现象挑战了当时主导的“神经论”。Bayliss和Starling认为盐酸可能使小肠粘膜产生了一种化学物质,该种物质随着血液被运送到胰腺,最终引起胰液分泌。为了证实这一设想,Starling把一段狗空肠粘膜制备成粗提液,注射到另一只狗的静脉中去,结果引起了明显的胰液分泌。由此,他们将其中能引起胰液分泌的化学物质命名为肠促胰液素(secretin)[2]。
肠促胰液素的发现,开创了一个全新的学科领域——内分泌学。Bayliss和Starling的研究证实了除神经系统外,机体内还存在着一个以化学物质传递调节远处器官活动的途径。1905年,Hardy将这类化学物质命名为“激素”(hormone, 源于希腊语词根hormao,意思是刺激)。在这之后,各种激素如雨后春笋般地被接连发现。1906年,Edkins发现了胃泌素(gastrin) [3],随后,胆囊收缩素(cholecystokinin)、肠抑胃素(enterogastrone)、肠降血糖素(incretin)、尿抑胃素(urogastrone)、促十二指肠素(vilikinin duocrinin)等一系列激素被相继地报道,支持了Bayliss和Starling的内分泌学理论。
无独有偶,早在1850年,著名的法国实验生理学家Bernard就曾发现了关于酸性食糜进入小肠引起胰液分泌的现象,但没有引起世人的注意。而后巴甫洛夫实验室对此的研究更为深入。1894年,巴甫洛夫的一个学生Dolinski再现了这个现象:切断双侧迷走神经和双侧内脏大神经以及损坏延髓后,仍然会出现胰液分泌。但是巴甫洛夫和他的学生都是“神经论”的忠诚卫道士,他们坚持神经对于消化液分泌的绝对控制。巴甫洛夫一个移居加拿大的学生Babkin回忆起他导师当时的懊恼之情:“他一言不发地走出实验现场回到书房。过了半小时后,他又回到实验室来,深表遗憾地说:自然,人家是对的。很明显,我们失去了一个发现真理的机会!”
更为不走运的是另一个法国生理学家Wertherimer,就在Bayliss和Starling公布重大发现的前一年,他做了相同的实验,可惜的是,与巴甫洛夫殊途同归,他也认为小肠和胰腺之间存在难以彻底切除的局部神经反射。
美国石油大亨洛克菲勒说:“如果你要成功,你应该朝新的道路前进,不要跟随被踩烂了的成功之路。”在科学研究中更是行路难,开路更难。纵观古今,权威理论有它的普适性和前瞻性,但同样有它的局限性。在面对“权威的科学“与”科学的权威”的两难抉择时,Bayliss和Starling在一百多年前就已经给出了答案。
2. 凝视沧海的碧波:肠抑胃素的发现
肠抑胃素,“enterogastrone”,是20世纪早期内分泌学标杆性的发现之一,却鲜有人知道它是由中国人发现并命名的。
1886年,Ewald和Boas观察到,位于小肠上部的未消化脂肪会抑制胃动力的活性。之后,巴甫洛夫和他的学生发现,脂肪对于胃液的分泌也有相似的抑制作用。但由于当时巴甫洛夫的神经学说占绝对主导地位,这一现象便自然地被认为完全由神经支配。
1927年,北京协和医学院生理系主任林可胜先生发现主胃中的脂肪可以抑制自体移植的胃囊分泌。据此,他怀疑这种抑制现象是由体液,而非由神经调节的。同年,冯德培从复旦大学生物学院转入北京协和医学院生理系,师从林可胜先生。1929年,冯德培与林可胜等在《Chinese Journal ofPhysiology》上共同发表了题为:“On the mechanism of the inhibitionof gastric seceretion by fat”的研究论文[4]。他们的研究结果表明,完全不受神经支配、移植的胃囊仍然受到主胃中脂肪的抑制,他们认为抑制胃液分泌的并非是进入循环的某个脂肪代谢产物,并据此推测,在进食脂肪后,肠胃系统可能存在着一种与刺激胃分泌激素相抗衡的肠胃抑制激素,将其命名为“enterogastrone”,即肠抑胃素。Enterogastrone 一词是由三个成分组合而成的合成词。“entero- ”表示“肠的”,“gastric”表示“胃的”,“one (s) ”表示可独立行使某种功能的最小单元[5]。。这一结果随后被Zetteiman和Ivy的研究证实。
林可胜先生的研究团队坚信这种物质由小肠粘膜分泌,随后进入血液,并最终作用到胃部,抑制了胃液的分泌。1932年,他们成功地制备了具有抑制胃分泌活性的小肠粘膜提取物,并针对肠抑胃素进行了系统的跟踪研究[6-8],当时在北京协和医学院进修的年轻日本学者小坂隆雄(T. Kosaka),与林可胜一起署名发表了关于肠抑胃素的学术研究论文,被追捧为“日本肠胃激素之父”。
囿于当时科学技术的限制,“Enterogastrone” 的含意并非指单一物质,应是涵盖被后人解密的包括促胰液素、胆囊收缩素和抑胃肽等在内的诸多激素混合物。可惜的是,抗日战争的爆发,使得在这方面的研究戛然而止。1932年,日军意欲染指华夏,长城战役爆发,林可胜先生即带领医疗队参与救援。七七事变之后,他投笔从戎,参加了红十字救护队。随后,太平洋战争爆发,北京协和医学院被迫关闭。尽管战事频发,科研环境恶劣,直到1965年之前,中国学者仍在 “肠抑胃素”的处女地上独自耕耘。
3. 花繁锦簇迷人眼:胃肠激素的发展与脑肠肽的发现
20世纪初叶,多种激素的生理功能被揭示,支持了内分泌学说。然而,尽管Edkins在1906年就发现了胃泌素[3],由于当时没有得到纯化的胃泌素,他的发现只能停摆在“胃泌素假说”(gastrinhypothesis)层面。
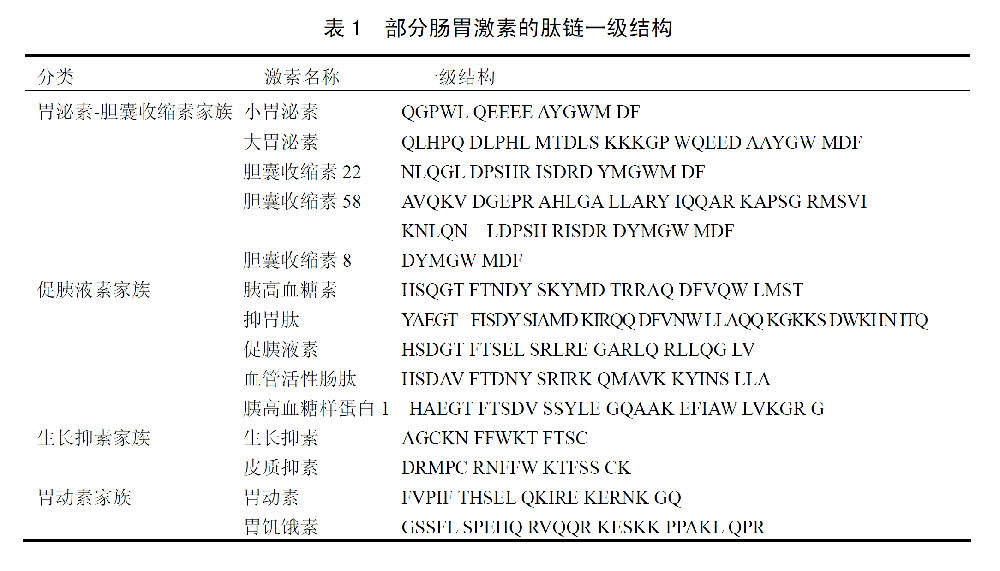
围绕“胃泌素假说”的争论一直持续到了1959年。Gregory和Tracy运用葡聚糖凝胶色谱法,首次从狗的肠胃组织中分离纯化得到了一个十七肽的胃泌素单体分子。接着,他们又相继得到了人源十七肽胃泌素以及更大分子量的前胃泌素(progastrin)和前胃泌素原(preprogastrin) [9]。其他肽类激素,如胆囊收缩素(cholecystokinin,CCK)、促胰液素(Secretin)和血管活性肠肽(vasoactive intestinalpeptide,VIP)等也都一一被相继纯化。其中,由小肠粘膜K细胞分泌的43肽分子—抑胃肽(Gastricinhibitory polypeptide,GIP)显示出与“肠抑胃素”相同的生理功能性质[10]。胆囊收缩素、生长抑素(somatostatin)和促胰液素等激素也被相继报导类似“肠抑胃素”的生理活性。迄今,被发现的胃肠肽类激素多达40余种(表一)。
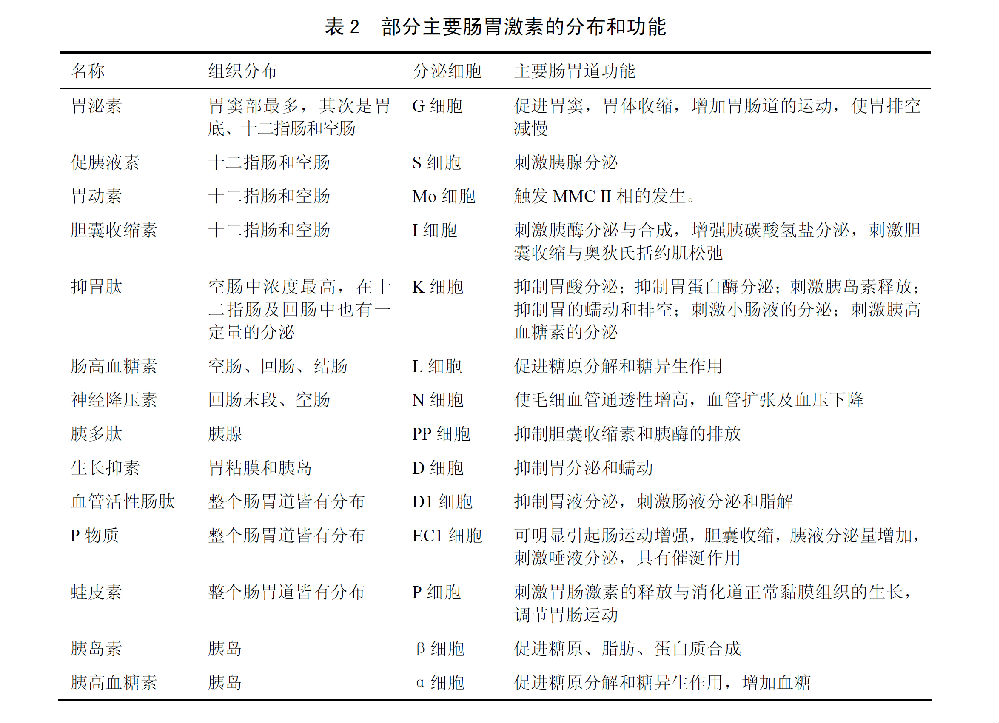
上世纪50年代,Berson和Yalow创立的“放射免疫测定方法”(radioimmunoassay, RIA),突破了对微量胃肠激素测定的技术瓶颈[11]。1970年,日本内分泌生理学巨儒矢内原升(N. Yanaihara)利用合成的C肽,优化了“放射免疫测定方法”,并发展成为探索肽类激素生化性质和生理功能的一种常规手段, 同时已被广泛应用于食品工业微量激素或添加物的检测[12]。技术上的革新使得越来越多具有重要生理功能作用的激素被发现(见表二),以至于似乎形成了“体液调节”与“神经调节”两块互不关联的独立分野。然而,伴随脑肠肽的发现,“体液调节”与“神经调节”又似乎渐渐地走向了统一。
1931年,两个美国生理学家Ulf von Euler和Gaddum在研究体内乙酰胆碱分布时意外发现,马的脑和小肠提取物都可刺激兔的肠平滑肌收缩,他们将其命名为P物质(Substance P)[13]。40年后,这种物质被证明是一个由11个氨基酸残基组成的多肽分子。接着,从脑和胃肠道还陆续分离神经降压素,生长抑素,胆囊收缩素,促胰液素等肽类物质。借助放射免疫检测和免疫组化的方法还发现了一些微量肽类物质在脑和胃肠道呈表达差异性共分布。如在肠道中存在脑啡肽,大脑中也发现了血管活性肠肽和胃动素等典型的胃肠激素。许多肠胃激素对中枢神经系统具有调控作用:兔脑中注射胆囊收缩素可使胆囊内压力降低;狗侧脑室注射生长抑素可使胃收缩加强。这些发现使胃肠分泌和胃肠动力调节机制的理论上升到了一个新阶段,激素的释放方式也打破了内分泌学的传统认知,浮现了神经分泌等新概念。同样,伴随脑肠肽的发现引申出了“脑肠轴”理论。
再以胆囊收缩素为例,胆囊收缩素分泌于食物进入胃肠道之后,一方面CCK刺激迷走神经传入纤维发往脑干孤束核,通过中枢,阻止摄食和胃排空,另一方面,CCK促进胰液和胆盐分泌,加速消化小肠中的食物。胆囊收缩素的双重作用使得两个消化步骤得以衔接和配合。
胃饥饿素(ghrelin)主要由胃底P/D1细胞和胰ε细胞分泌,其分泌量在餐前上升,通过激活下丘脑的NPY/AgRP神经元,产生饥饿感 [14]。神奇的是,另一种由胃和小肠分泌的激素——肥胖抑素(Obestatin),它与胃饥饿素由同一个基因编码,却行使了相反的功能[15]。
1950年,Jackson实验室报道,在一个鼠群中,会随机出现突变的肥胖小鼠[16]。1994年,Rockefeller大学的Jeffrey成功地克隆到了一个与肥胖相关的基因(obese,ob),由该基因编码的蛋白被命名为瘦素(leptin)[17],随后,另一种同样引起病态肥胖老鼠的突变基因(db/db)被认为编码了瘦素的受体[18]。瘦素主要由脂肪组织分泌,脂肪组织增加时,瘦素的分泌量也会随之增加。在胃黏膜上皮细胞、胎盘等其他组织中也检测到了瘦素的分泌。瘦素可以通过血脑屏障,直接抑制下丘脑NPY/AgRP神经元和激活POMC/αMSH神经元,产生饱腹感,抑制摄食行为并增加能量消耗[19](参见图1)。当将瘦素注入ob基因突变的肥胖症小鼠后,该突变小鼠会减负脂肪,回到正常体重。
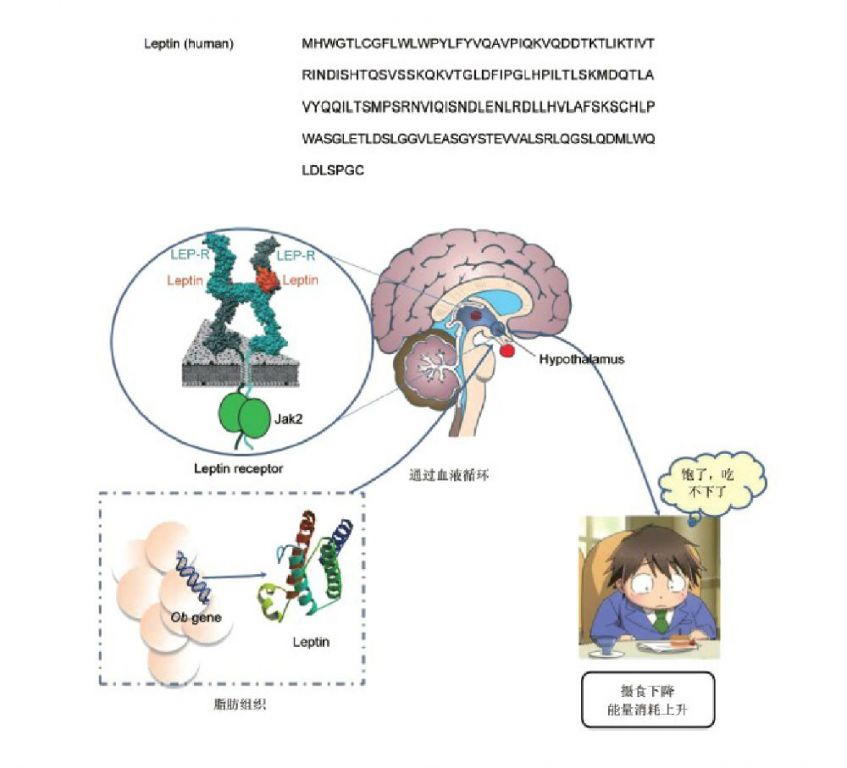
那么,归纳瘦素的奇妙,它与生长激素释放肽共享对NPY/AgRP神经元的调控通路,差异体现在前者抑制、后者激活NPY/AgRP神经元,导致了截然相反的生理功能现象。瘦素在很大程度上与肥胖抑素有着异曲同工的功效。
从1929年“肠胃抑素”叩世至1969年的40年间,独由中国学者贡献的关于“肠胃抑素”的研究论文不足20篇。然而,始于上世纪70年代至90年代的20余年间,在国际上发表的相关肠胃激素研究论文陡升至数千篇的“量变”腾图里,以及接踵而至的一波波肠胃激素产业化的“质变”浪潮中却难寻中国人参与博弈的踪迹。
4. 乍暖还寒犹未定:胃肠激素产业化道路
英国文艺复兴时期的哲学家培根说过“科学真正的、合法的目标不外乎是把新的发现和新的力量惠赠给人类生活”。在促胰液素被发现之后的几十年里,对于胃肠激素的研究似乎仅限于生理和病理机制的范畴。20世纪60年代,蛋白质研究步入人工合成时代。1967年,Konturek根据胃泌素C端的序列,合成了一个被命名为五肽的胃泌素(pentagastrin)[21],因该合成肽同样能引起胃液的分泌,被迅即用于测定胃的分泌活力。
与内源性胆囊收缩素不同,人工合成的胆囊收缩素-4(CCK-4)可特异性地作用于中枢神经系统。它作为诱导焦虑的药物已被广泛应用于研发新型降压药的病理动物模型构建[22]。
1973年,Brazeau等从绵羊下丘脑提取到了生长抑素,该激素随后被发现在胃肠道和脑内皆有分布,具有抑制胃分泌和蠕动以及在下丘脑/垂体中抑制促生长素释放的作用[23]。瑞士雪兰诺公司(Serono S.A)将其开发成静脉注射药物—思他宁,用于临床上对急性胃或十二指肠溃疡出血的治疗及对胰、胆和肠瘘的辅助治疗,被誉为最为成功的商品化制药典范。
瑞士诺华制药公司(Novartis Pharma Stein AG)开发的善宁(Sandostatin)则是基于生长抑素改造而来的八肽药物。善宁对生长激素、胰高血糖素和胰岛素的抑制能力均强于天然的生长抑素。相对于生长抑素的2-3分钟半衰期,善宁的持久力可达90分钟之久[24]。善宁现已被用于治疗临床肢体肥大症、类癌综合症、肝脏和肾脏的多囊症。
索马杜林(Somatuline)是另一由生长抑素改造而来的药物,由法国易普森公司(Ipsen International GmbH)生产,与善宁类似,索马杜林也表现出了较长的半衰期,并用于治疗神经内分泌肿瘤和肢体肥大症[25]。
然而,肽类激素的普惠前景有其难克的先天性缺憾。其一,肽类激素的生产较为困难,使得药物的成本居高不下;其二,肽类药物的静脉给药方式,远不及口服的经济与便捷;其三,肽类激素的半衰期都较短,不得不保持一个较高的给药频率,加重了患者的支付。
瘦素被认为是最具有产业化潜力的多肽之一。08年的一项测试显示,肥胖症患者使用天然瘦素的类似物—普兰林肽/美曲普汀(metreleptin)复方制剂治疗24周后,体重平均下降了12.7%。2013年5月,美国FDA将本土Amylin公司开发的美曲普汀列入计划审批的新药。
束语:中国自古就不缺创新思想和原创果实,且不提国人常沾沾自喜的“四大发明”,近代更不乏冯德培、林可胜等开创“enterogastrone”先河研究的典例,然而,经受异邦星移斗转、瞬息万变的海啸般冲击,这样似曾相识的荣光或早已淡漠,褪色在凝重中国科学史的尘灰记忆中……。“中国梦”的实现离不开创新,在历史厚重、人口环境、制度经济伤痕累累的背景下,这段远非平坦的征程似乎方才开始。回望闪耀在中国历史的群“新”璀璨,与其扼腕叹息焕发寻道精神的老一辈科学家们远去的身影,留待吾辈后继者的何止“三省吾身”?
其一、珍惜原始创新的孕育生态:固然,“春风拂面,人心向暖”是政策“绿灯”造就的积极局面。“深化体制改革、解放科研束缚”绝不是一句标语式的口号,如果将“科技体制”形象化为“为科研服务的看门人”,若开启“科学大门”的钥匙不在科研工作者的手中,原始创新难免会“自慰式忽悠”,“肥水流入外人田”,“墙内开花墙外香”,孕育的“生态”终究是“送礼体面过人的中秋月饼”。
其二、科学家的“井冈山”:冯德培先生晚年曾语重心长地教导他的学生:“毛泽东有井冈山红色政权根据地,方能打下江山,建立了新中国。科研人员在探索未知世界的征程中同样要建立起自己的“井冈山根据地”,事业发展才有立身之本”。冯德培先生本人早年虽没有与他的同仁们一道继续“肠抑胃素”的深究,他转战在“神经肌肉接头生理学”领域构筑起的高地,足以被铭刻。姑尚且不论我国科研是否已处于“百花齐放”的局面,若一味追崇“小炉匠敲打修补式”或“熊瞎子掰苞谷式”研究,热衷“浑水捞鱼”[26]……,其隐殇岂限于科研大军对“诺奖愈渴望愈无望”的破局?
其三、科研也要“嫁对郎”:“教好书、选好题、做好人、说真话。”是陈宜张先生对“如何做好学者”的肺腑感言。他特别强调,选好题最具挑战性。直白的说,要知晓前人做过了什么,别人还没做什么,关键是我能做什么。如同“嫁人”首先要“谈感情”,但“青春期”的“表面恩爱”只能是一时的“激情”,若要“地老天长”,还得看“人品,物质基础,发展潜力……”,科研亦不如是?
其四,……
但愿在经济快轨的驰行中,中国的科研也能登上这趟高铁,让更多的“肠抑胃素”在中国的土地生根发芽、枝繁叶茂……。
参考文献:
1 Konturek PC, KonturekSJ. The history of gastrointestinal hormones and the Polish contribution toelucidation of their biology and relation to nervous system. J PhysiolPharmacol 2003; 54 Suppl 3: 83-98.
2 Bayliss WM,Starling EH. The mechanism of pancreatic secretion. J Physiol 1902; 28(5):325-353.
3 Edkins JS. Thechemical mechanism of gastric secretion. J Physiol 1906; 34(1-2): 133-144.
4 Feng TP, Hou HC, Lim RKS. On the mechanismof the inhibition of gastric seceretion by fat. Chin J Physiol 1929; 3, 371.
5 吉永华. 凝视曾经沧海的碧波—记冯德培先生等开启“Enterogastrones”先河的奠基性贡献. 生理学报, 2007, 59(6):736–737.
6 Kosaka T, Lim RKS. Demonstration of the humoral agent in fat inhibition ofgastric acid secretion. Proc Soc Exp Biol Med 1930.
7 Kosaka T, Lim RKS, Ling SM, LiuAC. On the mechanism of the inhibition of gastric seceretion by fat. Agastric-inhibiting agent abtained from the intestinal mucosa. Chin J Physiol1932; 6: 107-126.
8 Lim RKS.Observation on the mechanism of the inhibition of gastric seceretion by fat. QJ Exp Physiol 1933; 23: 263-268.
9 GregoryRA, Tracy HJ. The Constitution and Properties of Two Gastrins Extracted fromHog Antral Mucosa. Gut 1964; 5: 103-114.
10 Soon-ShiongP, Debas HT, Brown JC. The evaluation of gastric inhibitory polypeptide (GIP)as the enterogastrone. J Surg Res 1979; 26(6): 681-686.
11 YalowRS, Berson SA. Immunoassay of endogenous plasma insulin in man. 1960. Obes Res1996; 4(6): 583-600.
12 KannoT. Memorial to Dr. Noboru Yanaihara. Pancreas 2002; 24(3): 215–216.
13 US VE, Gaddum JH. An unidentifieddepressor substance in certain tissue extracts. J Physiol 1931; 72(1): 74-87.
14 AbizaidA, Horvath TL. Ghrelin and the central regulation of feeding and energybalance. Indian J Endocrinol Metab 2012; 16(Suppl 3): S617-626.
15 HassounaR, Zizzari P, Tolle V. The ghrelin/obestatin balance in the physiological andpathological control of growth hormone secretion, body composition and foodintake. J Neuroendocrinol 2010; 22(7): 793-804.
16 IngallsAM, Dickie MM, Snell GD. Obese, a new mutation in the house mouse. J Hered1950; 41(12): 317-318.
17 ZhangY, Proenca R, Maffei M, Barone M, Leopold L, Friedman JM. Positional cloning ofthe mouse obese gene and its human homologue. Nature 1994; 372(6505): 425-432.
18 KobayashiK, Forte TM, Taniguchi S, Ishida BY, Oka K, Chan L. The db/db mouse,a model for diabetic dyslipidemia: molecular characterization and effects ofWestern diet feeding. Metabolism 2000; 49(1): 22-31.
19 AhimaRS. Revisiting leptin's role in obesity and weight loss. J Clin Invest 2008;118(7): 2380-2383.
20 ZhangF, Basinski MB, Beals JM, Briggs SL, Churgay LM, Clawson DK, DiMarchi RD,Furman TC, Hale JE, Hsiung HM, Schoner BE, Smith DP, Zhang XY, Wery JP,Schevitz RW. Crystal structure of the obeseprotein leptin-E100. Nature 1997; 387(6629): 206-209.
21 Konturek SJ. Gastrin-like pentapeptideI.C.I. 50 123: a potent gastric stimulant in man. Am J Dig Dis 1967; 12(3):285-292.
22 EserD, Schule C, Baghai T, Floesser A, Krebs-Brown A, Enunwa M, de la Motte S,Engel R, Kucher K, Rupprecht R. Evaluation of the CCK-4 model as a challengeparadigm in a population of healthy volunteers within a proof-of-concept study.Psychopharmacology (Berl) 2007; 192(4): 479-487.
23 FlorioT, Schettini G. [Somatostatin and its receptors. Role in the control of cellproliferation]. Minerva Endocrinol 2001; 26(3): 91-102.
24 LustigRH, Hinds PS, Ringwald-Smith K, Christensen RK, Kaste SC, Schreiber RE, Rai SN,Lensing SY, Wu S, Xiong X. Octreotide therapy of pediatric hypothalamicobesity: a double-blind, placebo-controlled trial. J Clin Endocrinol Metab2003; 88(6): 2586-2592.
25 KvolsLK, Woltering EA. Role of somatostatin analogs in the clinical management ofnon-neuroendocrine solid tumors. Anticancer Drugs 2006; 17(6): 601-608.
26 刘志睿,吉永华. 秉持“水至清,则无鱼”:哲理盲点还是现实泥沼?2013年8月13日联合时报(CN31-0019),第63期第6版.
本文已见刊《生理学报》2013,65(5)和《生理通讯》2013,5(12),感谢吴彬博士和刘志睿博士在文章撰写过程中的协助。